Thermodynamik
Thermodynamik: Energie → Reaktionen
Thermos’ Dynamitofen: Energiejuwelen → Reaktionsglas
Zellen und Organismen brauchen Energie, um ihre Vitalfunktion zu erhalten. Sie ermöglicht, dass chemische Reaktionen stattfinden können, die Arbeit erfordern und nicht spontan erfolgen. Es findet also ein Energieumsatz statt (Wärmeübertragung, Arbeit). Die chemische Thermodynamik (Wärmelehre) beschäftigt sich mit diesen energetischen Effekten.
1/24
Thermodynamik
Chem. Bindungen (aus Nahrung)
Alchemistenkammer (mit Nahrung)
Die Energie stammt aus chemischen Bindungen und diese stammen wiederum aus der Nahrung.
2/24
Thermodynamik > System und Umwelt
System = Reaktionsraum
Kugel = Reaktion
Man kann bei Reaktionen 2 Räume unterscheiden: das System und die Umgebung. Als System wird der Reaktionsraum bezeichnet, den wir untersuchen wollen. Das System wird willkürlich gewählt, je nachdem, was uns interessiert.
3/24
Thermodynamik > System und Umwelt
Umgebung: alles andere
Umgebung: mit Energiejuwelen
Alles, was nicht zum System gehört, ist die sog. Umgebung. Damit ist theoretisch das gesamte Universum gemeint.
4/24
Thermodynamik > System und Umwelt
Offenes System: Mensch
Offene Vitrine: Menschenstatue
Es können 3 Systeme unterschieden werden, je nachdem, ob sie Stoffe und Energie mit ihrer Umgebung austauschen. Beim offenen System werden sowohl Energie als auch Stoffe mit der Umgebung ausgetauscht.
5/24
Thermodynamik > System und Umwelt
Geschlossenes System
Gehende geschlossene Glaskugel mit Pflanze
Beim geschlossenen System werden Energie, aber keine Stoffe mit der Umwelt ausgetauscht.
6/24
Thermodynamik > System und Umwelt
Isoliertes System (abgeschlossenes System)
Isolierter Thermotank (abgeschlossener Tank)
Beim isolierten oder abgeschlossenen System werden weder Energie noch Stoffe mit der Umwelt ausgetauscht. Die Gesamtenergie bleibt konstant. Es greift der 1. thermodynamische Hauptsatz.
7/24
Thermodynamik > Energie
Energie: “Währung” für Arbeit (W)
Energiejuwel: Alchemisten zahlen für Arbeitsochse (W-Helm)
Energie kann als Fähigkeit eines Systems bezeichnet werden, Arbeit zu verrichten. “Investiert” es Energie in Arbeit (die Bewegung von Objekten), verringert sich die Energie des Systems.
8/24
Thermodynamik > Energie
Energie: Speicherform der Wärme (Q)
Energiejuwel: Feuer(-Qualle)
Energie kann auch als Speicherform der Wärme bezeichnet werden oder als die Fähigkeit eines Systems, Wärme abzugeben.
9/24
Thermodynamik > Energie
Joule (J)
Energie-Juwelen
Die Einheit der Energie ist Joule. 4,184 Joule (J) entsprechen einer Kalorie (cal).
10/24
Thermodynamik > Energie
Power bzw. Leistung (P)
Power-Leitungen
P vom Englischen Power. Es bezeichnet die umgesetzte Energie pro Zeitspanne und kommt in vielen Formeln vor.
11/24
Thermodynamik > Energieformen
Innere Energie U = Summe aller Energieformen im System
Innere Energie des Uhu = Energiekugeln in sich
Es gibt verschiedene Energieformen (s. unten), die in Summe als innere Energie des Systems bezeichnet werden (U).
12/24
Thermodynamik > Energieformen
Wärmeenergie Q
Feuerqualle gibt Uhu Energie
Die Wärmeenergie wird im Englischen auch heat genannt, im Deutschen alternativ thermische Energie. Die Wärmemenge gibt an, wie viel thermische Energie von einem Körper auf einen anderen Körper übertragen wird.
13/24
Thermodynamik > Energieformen
Potenzielle Energie
Po-Energiequelle
Die potentielle Energie eines Körpers besteht aufgrund seiner Lage in einem Energiefeld oder aufgrund seines Zustands (z.B. Kompression einer Feder). Arbeit muss aufgewendet werden, um die potenzielle Energie von Objekten zu erhöhen.
14/24
Thermodynamik > Energieformen
Kinetische Energie
Chinesische Energiekugel
Bewegungsenergie eines Körpers.
15/24
Thermodynamik > Energieformen
Chemische Energie
Alchemisten-Hut
Diese Energie ist in chemischen Verbindungen gespeichert und kann bei chemischen Reaktionen freigesetzt werden. Sie wird durch die räumliche Position der kleinsten Teilchen bestimmt. Bei chemischen Reaktionen wird sie meist in Form von Wärme frei (z.B. Reaktion von ATP zu ADP + P(inorganisch) durch Spaltung der Phosphatbindung).
16/24
Entropie
Entropie S = Ausbreitung von Energie / Unordnung
Tropen-Schlange = Explosion
Entropie (S) beschreibt die Ausbreitung von Energie bzw. die Unordnung eines Systems auf Teilchenebene. Es beschreibt damit auch die Wahrscheinlichkeit, wie sich Teilchen in einem System verhalten. Je größer die Entropie, desto größer die Unordnung. Thermos will sein Haustier auf maximale Größe (Unordnung) anfüttern.
17/24
Entropie
Entropie im Universum steigt (Systeme “streben” nach Entropie)
Splitter steigt in die Luft
In der Natur nimmt die Entropie niemals ab. Die Entropie nimmt zu oder bleibt konstant. Systeme “streben” nach maximaler Entropie bzw. Unordnung. Dieses “Streben” nach Entropie (die Zunahme der Entropie) kann sogar eine chemische Reaktion antreiben.
18/24
Entropie
↑ Entropie → ↑ Temperatur, ↑ Teilchen (Mol), ↑ Volumen
Tanzende Tropenfrüchte → Feuer der Explosion, viele Früchte und Molche, “Volllaufen”
Je höher die Temperatur, je mehr Teilchen, je höher das Volumen, desto höher die Entropie oder Unordnung. T, Mol und V sind also proportional zur Entropie.
19/24
Entropie
ΔS = ΔQ / ΔT
Dreieck neben Schlange = Splitter-Feuerqualle / Splitter Tasmanischer Temperaturteufel
Bei Reaktionen interessiert uns die Änderung der Entropie (ΔS). Nimmt ein System Wärmeenergie auf, steigt die Entropie (und umgekehrt). Bei irreversibel ablaufenden Prozessen (z.B. Verbrennung eines Stoffes), nimmt die Entropie immer zu.
20/24
Entropie
J/K
Juwel / Kelvin-Unterwäsche
Die Einheit der Entropie ist Joule/Kelvin.
21/24
Entropie
Gasförmige Substanzen = hohe Entropie
Wolke = über Tropenschlange
Die Teilchen im Gas sind “sehr ungeordnet” (s. Aggregatzustände).
22/24
Entropie
Flüssige Substanzen = moderate Entropie
Regen = fällt von Wolke
Flüssigkeit hat eine geringere Entropie als Gas, weil die Teilchen aufgrund von intermolekularen Kräften zueinander geordneter sind.
23/24
Entropie
Feste Substanzen = niedrige Entropie
Eis = auf Boden
Bei festen Substanzen ist die Teilchenstruktur organisiert (z.B. in einem Kristallgitter).
24/24
schließen

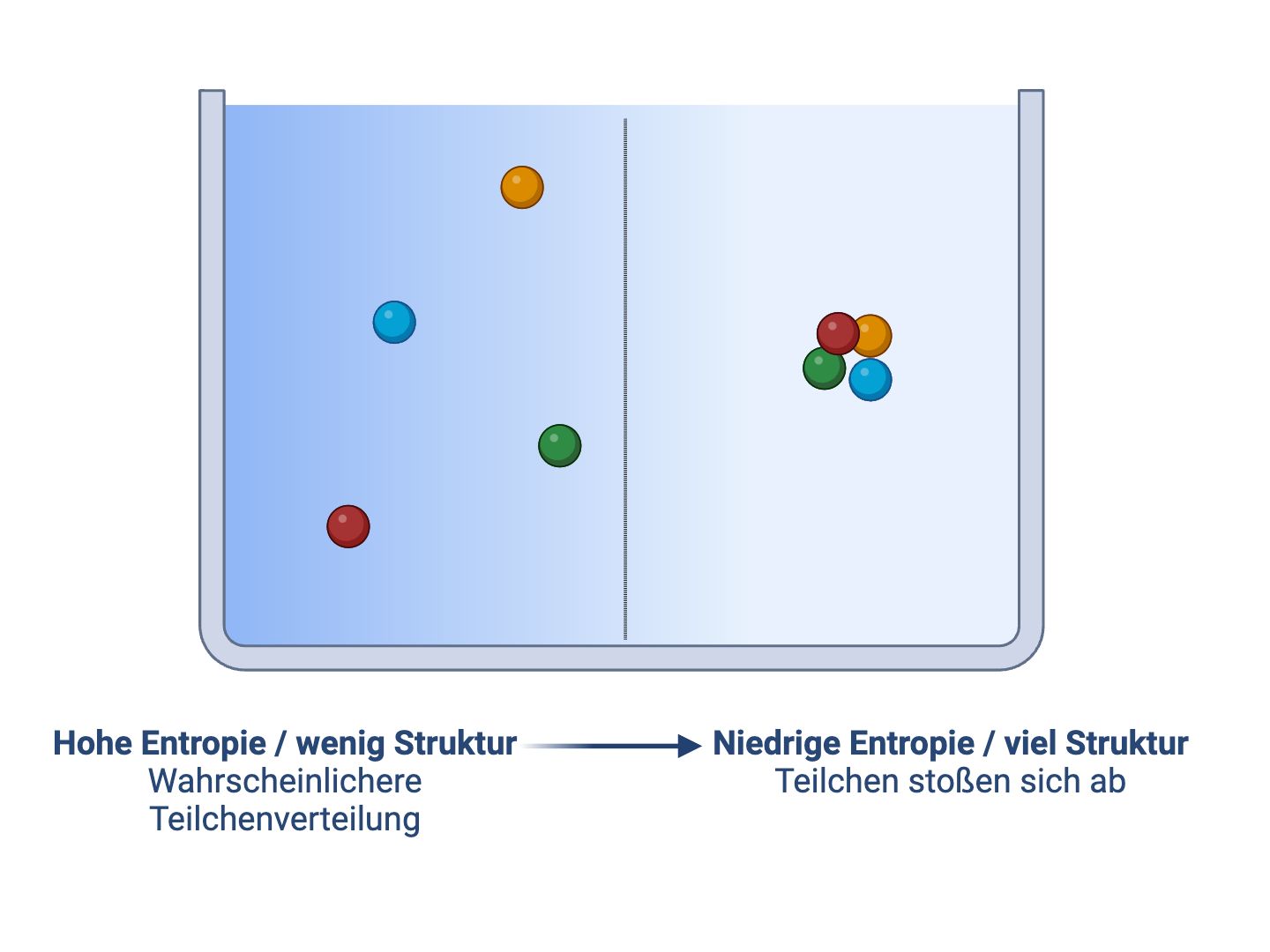
Die vier Teilchen in diesem geschlossenen System können sich in zahllosen Varianten “chaotisch” im Raum verteilen. Es gibt nur wenige strukturierte Anordnungen im Raum. Es ist viel wahrscheinlicher, dass sich die Teilchen im Raum verteilen..
fAsdnn34#SD6%4mgLS9(#k-mn
https://www.meditricks.de/wp-content/plugins/meditricks-mt-quiz/include/
n
75363
Was ist Ankizin?
Ankizin ist ein Projekt der AG Medizinische-Ausbildung bvmd e.V.
Es ist das größte non-profit, studentisch organisierte Anki-Projekt im deutschsprachigen Raum.
Ziel ist die Umsetzung des gesamten notwendigen Wissens für alle medizinischen Staatsexamina.
In freundlicher Kooperation bieten wir im Ankizin-Deck passgenau unsere Merkhilfen in den jeweiligen Anki-Karten an. Die so verknüpften Fragen kannst Du mit freundlicher Genehmigung der bvmd auch hier als Quiz ansehen.
Du findest alle Inhalte auch im Ankizin-Deck in Anki.
Es ist das größte non-profit, studentisch organisierte Anki-Projekt im deutschsprachigen Raum.
Ziel ist die Umsetzung des gesamten notwendigen Wissens für alle medizinischen Staatsexamina.
In freundlicher Kooperation bieten wir im Ankizin-Deck passgenau unsere Merkhilfen in den jeweiligen Anki-Karten an. Die so verknüpften Fragen kannst Du mit freundlicher Genehmigung der bvmd auch hier als Quiz ansehen.
Du findest alle Inhalte auch im Ankizin-Deck in Anki.




1
Thermodynamik
Thermos’ Dynamitofen: Energiejuwelen → Reaktionsglas
Zellen und Organismen brauchen Energie, um ihre Vitalfunktion zu erhalten. Sie ermöglicht, dass chemische Reaktionen stattfinden können, die Arbeit erfordern und nicht spontan erfolgen. Es findet also ein Energieumsatz statt (Wärmeübertragung, Arbeit). Die chemische Thermodynamik (Wärmelehre) beschäftigt sich mit diesen energetischen Effekten.
alles
anzeigen
2
Thermodynamik
Alchemistenkammer (mit Nahrung)
Die Energie stammt aus chemischen Bindungen und diese stammen wiederum aus der Nahrung.
alles
anzeigen
3
Thermodynamik > System und Umwelt
Kugel = Reaktion
Man kann bei Reaktionen 2 Räume unterscheiden: das System und die Umgebung. Als System wird der Reaktionsraum bezeichnet, den wir untersuchen wollen. Das System wird willkürlich gewählt, je nachdem, was uns interessiert.
alles
anzeigen
4
Thermodynamik > System und Umwelt
Umgebung: mit Energiejuwelen
Alles, was nicht zum System gehört, ist die sog. Umgebung. Damit ist theoretisch das gesamte Universum gemeint.
alles
anzeigen
5
Thermodynamik > System und Umwelt
Offene Vitrine: Menschenstatue
Es können 3 Systeme unterschieden werden, je nachdem, ob sie Stoffe und Energie mit ihrer Umgebung austauschen. Beim offenen System werden sowohl Energie als auch Stoffe mit der Umgebung ausgetauscht.
alles
anzeigen
6
Thermodynamik > System und Umwelt
Gehende geschlossene Glaskugel mit Pflanze
Beim geschlossenen System werden Energie, aber keine Stoffe mit der Umwelt ausgetauscht.
alles
anzeigen
7
Thermodynamik > System und Umwelt
Isolierter Thermotank (abgeschlossener Tank)
Beim isolierten oder abgeschlossenen System werden weder Energie noch Stoffe mit der Umwelt ausgetauscht. Die Gesamtenergie bleibt konstant. Es greift der 1. thermodynamische Hauptsatz.
alles
anzeigen
Extra Info / Trivia
Man könnte Energie auch als Währung der Biologie bezeichnen. Die Arbeit muss mit Energie bezahlt werden.
Arbeit kennzeichnet einen Vorgang oder Prozess (Prozessgröße). Energie beschreibt hingegen den Zustand eines Körpers (Zustandsgröße). Man kann auch von einer Erhaltungsgröße sprechen, da sich ihr Betrag in einem abgeschlossenen System nicht ändert.
Man könnte Energie auch als Währung der Biologie bezeichnen. Die Arbeit muss mit Energie bezahlt werden.
Arbeit kennzeichnet einen Vorgang oder Prozess (Prozessgröße). Energie beschreibt hingegen den Zustand eines Körpers (Zustandsgröße). Man kann auch von einer Erhaltungsgröße sprechen, da sich ihr Betrag in einem abgeschlossenen System nicht ändert.
8
Thermodynamik > Energie
Energiejuwel: Alchemisten zahlen für Arbeitsochse (W-Helm)
Energie kann als Fähigkeit eines Systems bezeichnet werden, Arbeit zu verrichten. “Investiert” es Energie in Arbeit (die Bewegung von Objekten), verringert sich die Energie des Systems.
alles
anzeigen
9
Thermodynamik > Energie
Energiejuwel: Feuer(-Qualle)
Energie kann auch als Speicherform der Wärme bezeichnet werden oder als die Fähigkeit eines Systems, Wärme abzugeben.
alles
anzeigen
10
Thermodynamik > Energie
Energie-Juwelen
Die Einheit der Energie ist Joule. 4,184 Joule (J) entsprechen einer Kalorie (cal).
alles
anzeigen
11
Thermodynamik > Energie
Power-Leitungen
P vom Englischen Power. Es bezeichnet die umgesetzte Energie pro Zeitspanne und kommt in vielen Formeln vor.
alles
anzeigen
11/24
12
Thermodynamik > Energieformen
Innere Energie des Uhu = Energiekugeln in sich
Es gibt verschiedene Energieformen (s. unten), die in Summe als innere Energie des Systems bezeichnet werden (U).
alles
anzeigen
13
Thermodynamik > Energieformen
Feuerqualle gibt Uhu Energie
Die Wärmeenergie wird im Englischen auch heat genannt, im Deutschen alternativ thermische Energie. Die Wärmemenge gibt an, wie viel thermische Energie von einem Körper auf einen anderen Körper übertragen wird.
alles
anzeigen
14
Thermodynamik > Energieformen
Po-Energiequelle
Die potentielle Energie eines Körpers besteht aufgrund seiner Lage in einem Energiefeld oder aufgrund seines Zustands (z.B. Kompression einer Feder). Arbeit muss aufgewendet werden, um die potenzielle Energie von Objekten zu erhöhen.
alles
anzeigen
15
Thermodynamik > Energieformen
Chinesische Energiekugel
Bewegungsenergie eines Körpers.
alles
anzeigen
16
Thermodynamik > Energieformen
Alchemisten-Hut
Diese Energie ist in chemischen Verbindungen gespeichert und kann bei chemischen Reaktionen freigesetzt werden. Sie wird durch die räumliche Position der kleinsten Teilchen bestimmt. Bei chemischen Reaktionen wird sie meist in Form von Wärme frei (z.B. Reaktion von ATP zu ADP + P(inorganisch) durch Spaltung der Phosphatbindung).
alles
anzeigen
17
Entropie
Tropen-Schlange = Explosion
Entropie (S) beschreibt die Ausbreitung von Energie bzw. die Unordnung eines Systems auf Teilchenebene. Es beschreibt damit auch die Wahrscheinlichkeit, wie sich Teilchen in einem System verhalten. Je größer die Entropie, desto größer die Unordnung. Thermos will sein Haustier auf maximale Größe (Unordnung) anfüttern.
alles
anzeigen
18
Entropie
Splitter steigt in die Luft
In der Natur nimmt die Entropie niemals ab. Die Entropie nimmt zu oder bleibt konstant. Systeme “streben” nach maximaler Entropie bzw. Unordnung. Dieses “Streben” nach Entropie (die Zunahme der Entropie) kann sogar eine chemische Reaktion antreiben.
alles
anzeigen
Extra Info / Trivia
Anders gesagt: Der maximal unordentliche Zustand ist der wahrscheinlichste Zustand von Systemen.
Die vier Teilchen in diesem geschlossenen System können sich in zahllosen Varianten “chaotisch” im Raum verteilen. Es gibt nur wenige strukturierte Anordnungen im Raum. Es ist viel wahrscheinlicher, dass sich die Teilchen im Raum verteilen.
Anders gesagt: Der maximal unordentliche Zustand ist der wahrscheinlichste Zustand von Systemen.
Die vier Teilchen in diesem geschlossenen System können sich in zahllosen Varianten “chaotisch” im Raum verteilen. Es gibt nur wenige strukturierte Anordnungen im Raum. Es ist viel wahrscheinlicher, dass sich die Teilchen im Raum verteilen.
19
Entropie
Tanzende Tropenfrüchte → Feuer der Explosion, viele Früchte und Molche, “Volllaufen”
Je höher die Temperatur, je mehr Teilchen, je höher das Volumen, desto höher die Entropie oder Unordnung. T, Mol und V sind also proportional zur Entropie.
alles
anzeigen
20
Entropie
Dreieck neben Schlange = Splitter-Feuerqualle / Splitter Tasmanischer Temperaturteufel
Bei Reaktionen interessiert uns die Änderung der Entropie (ΔS). Nimmt ein System Wärmeenergie auf, steigt die Entropie (und umgekehrt). Bei irreversibel ablaufenden Prozessen (z.B. Verbrennung eines Stoffes), nimmt die Entropie immer zu.
alles
anzeigen
21
22
Entropie
Wolke = über Tropenschlange
Die Teilchen im Gas sind “sehr ungeordnet” (s. Aggregatzustände).
alles
anzeigen
23
Entropie
Regen = fällt von Wolke
Flüssigkeit hat eine geringere Entropie als Gas, weil die Teilchen aufgrund von intermolekularen Kräften zueinander geordneter sind.
alles
anzeigen
24
Entropie
Eis = auf Boden
Bei festen Substanzen ist die Teilchenstruktur organisiert (z.B. in einem Kristallgitter).
alles
anzeigen

Entropie - Die vier Teilchen in diesem geschlossenen System können sich in zahllosen Varianten “chaotisch” im Raum verteilen. Es gibt nur wenige strukturierte Anordnungen im Raum. Es ist viel wahrscheinlicher, dass sich die Teilchen im Raum verteilen..
Meditricks Schaubild, erstellt mit BioRender.com.
Meine Notizen
|
Rückmeldung
Unsere Meditricks wurden mit viel Liebe ersonnen, illustriert und vertont. Gib uns gerne Lob, Kritik über die Feedback-Funktion unter den Meditricks oder schreib uns – siehe Kontakt.
Gereift unter der Sonne Freiburgs. mit viel Liebe zum Detail ersonnen, illustriert und vertont. Wir übernehmen keine Haftung für nicht mehr löschbare Erinnerungen.




 Quint
Quint